 Rosario Muto
Rosario Muto
METALLI PESANTI:
ELENCO, INTOSSICAZIONE E CHELAZIONE
Attenzione ai miei commeneti sono evidenziato in rosso.
Quando parlano gli indottrinati dott. sembra che la chimica è una opinione di cui solo loro ne possono parlare facendo poi sempre riferimenti a bibliografia discutibile e antica di cui non c'è ne uno che è daccordo con quello che dice l'altro.

METALLI PESANTI: ELENCO, INTOSSICAZIONE E CHELAZIONE
Ultima modifica 20.12.2022
https://healthy.thewom.it/salute/metalli-pesanti/
- COSA SONO I METALLI PESANTI?
- COS’È L’INTOSSICAZIONE DA METALLI PESANTI?
- DOVE SI TROVANO?
- SINTOMI
- DIAGNOSI
- CHELAZIONE
- FONTI E BIBLIOGRAFIA
COSA SONO I METALLI PESANTI?
Benché non esista una definizione universalmente accettata, parlando di metalli pesanti si fa in genere riferimento a sostanze appartenenti alla categoria chimica dei metalli con densità, pesi atomici o numeri atomici relativamente elevati; ( no, è falsa informazione, ogni materia si scompone a secondo delle sue condizioni e lo fa sotto forma ionica, quindi ogni ione si lega all’ossigeno divenendo ossido, metallo pesante), i criteri utilizzati possono tuttavia variare a seconda dell’autore e del contesto.
In medicina, ad esempio, è stato proposto di includere elementi chimici con la spiccata attitudine a formare complessi molecolari all’interno delle cellule, condizione che comprende sostanze come selenio e arsenico e non solo, che non sono metalli (falso, sono metalli pesanti), sebbene ne condividano alcune proprietà fisiche e chimiche.
Molti dei metalli pesanti, come zinco, rame, cromo, ferro e manganese tutta la materia, qualsiasi materiale, sono essenziali per il corretto funzionamento del corpo, che tuttavia ne necessita solo quantità estremamente piccole (la distanza tra dose necessaria è tossica può essere sorprendentemente piccola).
I metalli pesanti più comunemente associati all’avvelenamento degli esseri umani sono (solo disinformazione, i metalli pesanti sono tutte quelle nanoparticelle di cui si legano all'ossigeno formando ossidi metallici)
- arsenico
- cadmio
- mercurio
COS’È L’INTOSSICAZIONE DA METALLI PESANTI?
L’intossicazione (o avvelenamento) da metalli pesanti è una condizione caratterizzata da un’eccessiva ( falso, anche in minima parte) esposizione a un metallo pesante, tanto da influire sulla normale funzione dell’organismo.
Esempi di metalli pesanti che possono causare tossicità includono piombo, mercurio, arsenico, cadmio e cromo e l’esposizione può avvenire attraverso
- dieta (cibo e liquidi),
- farmaci,
- ambiente (ad esempio durante il lavoro o il gioco).
I metalli pesanti possono entrare nel corpo
- attraverso la pelle (per contatto),
- attraverso i polmoni e le vie respiratorie in genere (per inalazione),
- per assorbimento tramite stomaco/intestino (per ingestione).
La tossicità può derivare da un’esposizione
- improvvisa e grave (acuta),
- o diluita, ma costante nel tempo (cronica).
Ad esempio i bambini piccoli sono più suscettibili agli effetti dell’esposizione al piombo perché soggetti ad un assorbimento aumentato, peraltro con un cervello ancora in via di sviluppo e quindi più sensibile agli effetti della sostanza.
Se piccole tracce sono innocue, ( non è vero, falso, anche una minima parte può essere letale, non dimentichiamo che il corpo umano è un enorme e complicatissimo laboratorio di chimica) dosi più elevate possono causare disturbi di gravità variabile: nausea, vomito, diarrea e dolore addominale sono sintomi comuni in caso di ingestione acuta di metalli, mentre l’esposizione cronica mostra sintomi diversi a seconda degli organi dove si verifica l’accumulo, oltre ad aumentare tipicamente il rischio di sviluppo di tumori. Sono possibili anche cambiamenti comportamentali e disturbi cognitivi quando ad essere interessato è il cervello.
I fattori principali che influenzano il rischio di tossicità annoverano
- età,
- peso corporeo,
- genetica,
- forma di esposizione,
- durata dell’esposizione,
- quantità di metallo,
- stato di salute generale.
DOVE SI TROVANO?
I metalli pesanti si trovano naturalmente nell’ambiente, talvolta anche in alcuni medicinali (falso, i medicinali sono metalli pesanti, sono idrocarburi) , integratori e alimenti e le stesse sostanze chimiche utilizzate nell’industria e nell’agricoltura possono contenere metalli pesanti, che possono poi finire nell’aria, nel suolo e nell’acqua.
Alla luce dell’ubiquità di queste sostanze è del tutto normale averne piccole tracce nell’organismo (ad esempio il riso è noto per accumulare l’arsenico), (falso, è il tipo di produttività che lo inquina)
I metalli pesanti entrano nel tuo corpo in modi diversi. Potresti respirarli, mangiarli o assorbirli attraverso la pelle. Poiché i metalli pesanti sono praticamente ovunque, è normale averne alcuni nel tuo corpo. Ma se troppo metallo pesante entra nel tuo corpo, può causare avvelenamento da metalli pesanti.
L’avvelenamento da metalli pesanti può portare a danni agli organi, cambiamenti comportamentali o difficoltà di pensiero e memoria. I sintomi dell’avvelenamento da metalli pesanti dipendono dal tipo di metallo, dalla quantità presente nel tuo corpo e dalla tua età. I bambini e i bambini non ancora nati hanno il rischio più elevato di gravi problemi di salute a lungo termine dovuti ai metalli pesanti.
Shutterstock/Microgen
Metalli pesanti e alimenti
Si noti che acquistando prodotti di provenienza sicura e controllata, e adottando una dieta varia e bilanciata, il rischio di intossicazione è sostanzialmente nullo.
L’arsenico può essere introdotto mediante:
- acqua contaminata,
- riso e prodotti da esso derivati (la fonte principale), per le spiccate capacità di accumulare il metallo a causa della crescita in acqua,
- cereali ed in particolare il frumento,
- in minor misura verdura e ortaggi.
Per la popolazione generale, con l’eccezione dei fumatori, la fonte principale di esposizione al cadmio è l’alimentazione, ad esempio:
- cereali e prodotti derivati
- verdura e ortaggi
- patate
- crostacei e molluschi.
Il mercurio è purtroppo un noto inquinante delle acque marine, dove si accumula progressivamente lungo la catena alimentare; ne sono quindi fonti particolarmente rilevanti tutti i frutti di mare e pesci e, in particolare, quelli di taglia grande (spada, tonno, luccio, …), senza dimenticare che il mercurio è anche nel cemento armato.
Il piombo è purtroppo un contaminante presente quasi ovunque nell’ambiente, soprattutto in tutti gli oggetti in vetro e ceramica e, dal punto di vista dietetico, può essere introdotto con:
SINTOMI
Arsenico
L’arsenico è utilizzato nella produzione di pesticidi, ma trova applicazione anche in contesti industriali.
Un’eccessiva esposizione acuta può causare
e più in generale complicazioni potenzialmente letali.
Tra gli apparati colpiti figurano:
- sistema nervoso centrale (encefalopatia, neuropatia periferica, demielinizzazione, …)
- pelle (strie ungueali bianche trasversali note come linee di Mees, eccessivo accumulo di liquidi, …)
- gastrointestinale (sintomi tipici da gastroenterite, come vomito, dolore addominale, febbre, diarrea, talvolta sanguinolenta).
Possono verificarsi anche ipotensione (pressione bassa), emolisi (distruzione massiva dei globuli rossi) e conseguente anemia.
In caso di avvelenamento cronico, possono comparire
- debolezza,
- dolori muscolari,
- brividie febbre.
Cadmio
L’insorgenza dei sintomi da avvelenamento da cadmio può essere ritardata da due a quattro ore dopo l’esposizione.
La forma acuta può causare
- affaticamento,
- mal di testa,
- nausea e vomito,
- crampi addominali,
- diarrea
- e febbre.
Il paziente potrebbe anche andare incontro a gravi complicazioni polmonari:
- perdita progressiva della funzione polmonare (enfisema),
- accumulo anomalo di liquido nei polmoni (edema polmonare)
- e ovviamente affanno (dispnea).
Alcuni soggetti possono presentare
- aumento della salivazione
- ingiallimento dei denti
- battito cardiacoaccelerato (tachicardia)
- anemia da carenza di ferro (che viene spiazzato nei globuli rossi)
- colorazione bluastra di pelle e mucose a causa dell’insufficiente apporto di ossigeno a questi tessuti (cianosi)
- alterazioni del senso dell’olfatto
e più in generali alterazioni della funzionalità
- epatica,
- renale,
- ossea (osteomalacia).
Mercurio
Il mercurio è utilizzato da assistenti dentali, igienisti e lavoratori chimici. Il mercurio può gravemente influenzare il funzionamento di
- polmoni,
- reni,
- cervello
- e/o la pelle.
I sintomi dell’avvelenamento da mercurio comprendono ad esempio
- affaticamento,
- depressione,
- grave sonnolenza (letargia),
- irritabilità,
- mal di testa.
I sintomi respiratori associati all’inalazione dei vapori di mercurio includono invece
- tosse,
- fame d’aria,
- senso di oppressione toracica o dolore bruciante al petto,
- distress respiratorio
ed eventualmente
- accumulo anomalo di liquido nei polmoni (edema polmonare)
- polmonite
- formazione anomala di tessuto fibroso (fibrosi).
L’avvelenamento acuto può indurre anche sintomi comportamentali e neurologici (eccessiva eccitabilità, irascibilità, mancanza di concentrazione e perdita di memoria) e a dosi elevate anche shock e danni cerebrali permanenti.
È comune lo sviluppo di movimenti involontari come movimenti a scatti, incontrollati, in associazione a movimenti più lenti e contorti (coreoatetosi).
Ulteriori sintomi possono comprendere
- polineuropatia (degenerazione dei nervi periferici),
- ridotta capacità di coordinare i movimenti volontari (atassiacerebellare)
- tremoridelle gambe e delle braccia e, in alcuni casi, della lingua e delle labbra
- convulsioni
- linguaggio confuso per cause neurologiche-motorie (disartria).
Sono noti alterazioni del comportamento tra cui la cosiddetta sindrome del cappellaio matto (eretismo) che si manifesta con:
- perdita di memoria,
- eccessiva timidezza,
- eccitabilità anomala
- e/o insonnia.
Molte persone colpite sperimentano infine
- disturbi sensoriali come problemi visivi e dell’udito, ma anche un’eccessiva sensibilità (iperestesia),
- alterazioni della pelle.
Il mercurio viene espulso principalmente attraverso l’urina e le feci.
Piombo
Gli effetti dell’avvelenamento da piombo variano a seconda dell’età dell’individuo e della quantità di metallo cui si viene esposti.
Nei bambini i sintomi di solito si sviluppano in un periodo di tempo da tre a sei settimane, con la comparsa di
- riduzione dell’attività (i bambini diventano meno giocosi, più goffi, irritabili e pigri,
- mal di testa,
- vomito,
- dolore addominale,
- mancanza di appetito (anoressia),
- stitichezza,
- disturbi del linguaggio (disartria),
- alterazioni della funzionalità renale,
- palloreconseguente ad una riduzione del ferro nei globuli rossi (anemia).
I sintomi neurologici associati alla sovraesposizione da piombo includono
- riduzione della capacità di coordinazione (atassia),
- danni cerebrali (encefalopatia),
- convulsioni,
- gonfiore del nervo ottico (papilledema),
- alterazione della coscienza.
Alcuni bambini affetti sviluppano problemi di apprendimento o comportamentali, come ritardo mentale e deficit selettivi nel linguaggio, nella funzione cognitiva, nell’equilibrio, nel comportamento e nel rendimento scolastico.
Negli adulti si osservano
- febbre,
- mal di testa,
- affaticamento,
- vomito,
- perdita di appetito (anoressia),
- dolore addominale,
- costipazione,
- dolori articolari,
- perdita di capacità acquisite di recente,
- perdita di coordinazione,
- svogliatezza,
- difficoltà a dormire (insonnia),
- irritabilità,
- alterazioni della coscienza,
- allucinazioni,
- convulsioni,
- aumento della pressione del sangue,
- lesioni agli organi riproduttivi,
- anemia,
- neuropatia periferica,
- lesioni cerebrali.
Il piombo può diventare fatale a dosi elevate; viene escreto nelle urine e nelle feci, tuttavia è possibile isolarlo anche in capelli, unghie e in diversi fluidi corporei come sudore, saliva e anche nel latte materno.
DIAGNOSI
Per la diagnosi di intossicazione da metalli pesanti è possibile ricorrere a esami di:
- sangue,
- urine,
- capelli,
- unghie,
Sangue e urine possono essere utili a valutare esposizioni acute, mentre gli altri tessuti sono in grado di testimoniare un’esposizione prolungata nel tempo; vale la pena notare che i sintomi potrebbero non essere necessariamente correlati ai livelli ematici, ad esempio il paziente potrebbe risultare gravemente provato eppure mostrare solo piccole tracce di metallo nel sangue.
A seconda delle manifestazioni possono risultare utili test ausiliari come ad esempio:
- emocromo(in caso di sospetta anemia)
- esami di funzionalità epatica,
- esami di funzionalità renale,
- elettrolitied in particolare:
- proteine nelle urine.
Radiografie e TC possono essere utili per la conferma diagnostica e/o per l’esclusione di altre patologie.
CHELAZIONE
Oltre alla necessaria interruzione dell’esposizione al metallo si può tentare di somministrare agenti chelanti, sostanze in grado di legare il metallo e consentirne l’eliminazione con l’urina. (Falso, attenzione che la chimica chelante lei stessa può essere oggetto tossico e difficile da rimuovere).
I principi attivi più usati a questo scopo sono
- Dimercaprolo
- EDTA
Gli agenti chelanti non sono purtroppo privi di effetti collaterali, ad esempio alcuni ioni metallici vengono ridistribuiti ad altri tessuti come il cervello, dove ne aumentano la neurotossicità; altri chelano oligoelementi essenziali (catturano cioè elementi utili e non solo quelli dannosi) producendo uno stato di carenza, mentre altri ancora possono indurre epatotossicità.
In alcuni casi potrebbe essere di beneficio anche la lavanda gastrica.
Parallelamente si porta in genere avanti anche un trattamento sintomatico e di supporto, ad esempio in caso di edema cerebrale (gonfiore del cervello) è necessario il trattamento con mannitolo (un agente diuretico) e farmaci corticosteroidi ( farmaci molto tossici letali), oltre ad un costante monitoraggio della pressione intracranica.
L’insufficienza renale può richiedere l’emodialisi.
FONTI E BIBLIOGRAFIA
- NIH
- MedLinePlus
- RareDiseases
- Heavy Metal Toxicity– Venkatraman Rajkumar; Vincent R. Lee; Vikas Gupta.
- ISS
AUTORE
laureato in Farmacia, PhD.
Laurea in Farmacia con lode, PhD in Scienza delle sostanze bioattive.
Fondatore del sito, si occupa ad oggi della supervisione editoriale e scientifica.
Rosario Muto















 e il parametro reticolare a = 361 pm.
e il parametro reticolare a = 361 pm. Un uso importante per lo zirconio sono i gusci di celle a combustibile all'uranio di Zircaloy nelle centrali nucleari. Questa lega è composta per circa il 90% di zirconio e piccole quantità di stagno, ferro, cromo o nichel, ma non deve contenere afnio. Il motivo per cui è stato scelto questo elemento è la sezione a bassa cattura già descritta per neutroni termici con elevata resistenza alla corrosione, che lo rende adatto anche come materiale da costruzione per impianti chimici, in particolare per parti di apparecchi speciali come valvole, pompe, tubi e scambiatori di calore. Come aggiunta di lega all'acciaio, aumenta anche la resistenza alla corrosione. Gli strumenti chirurgici sono fabbricati con leghe appropriate.
Un uso importante per lo zirconio sono i gusci di celle a combustibile all'uranio di Zircaloy nelle centrali nucleari. Questa lega è composta per circa il 90% di zirconio e piccole quantità di stagno, ferro, cromo o nichel, ma non deve contenere afnio. Il motivo per cui è stato scelto questo elemento è la sezione a bassa cattura già descritta per neutroni termici con elevata resistenza alla corrosione, che lo rende adatto anche come materiale da costruzione per impianti chimici, in particolare per parti di apparecchi speciali come valvole, pompe, tubi e scambiatori di calore. Come aggiunta di lega all'acciaio, aumenta anche la resistenza alla corrosione. Gli strumenti chirurgici sono fabbricati con leghe appropriate.
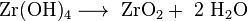
 Il composto di zirconio più importante è il biossido di zirconio ZrO2, un ossido molto stabile
Il composto di zirconio più importante è il biossido di zirconio ZrO2, un ossido molto stabile 

